荧光量子产率测定试剂盒 适合于生物偶联基团
| Ex (nm) | - | Em (nm) | - |
| 分子量 | - | 溶剂 | - |
| 存储条件 | 在零下15度以下保存, 避免光照 |
荧光量子产率测定试剂盒是美国AAT Bioquest生产的荧光染料,当荧光团吸收光子时,就会形成能量激发态。荧光团及其周围环境的确切性质,会影响该生物物种的形态,但结果是仍然是失活(能量损失)并返回基态。发生的主要失活过程是荧光(光子发射造成的能量损失)、内转换和振动弛豫(对周围环境的热量造成的非辐射能量损失)、与三重态流形交叉的系统间以及随后的非辐射失活。荧光量子产率是吸收的光子与通过荧光发射的光子之比。换句话说,量子产率给出了激发态被荧光而不是被另一个非辐射机制失活的可能性。该试剂盒提供了测定生物偶联物荧光量子产率的所有必要成分。该试剂盒针对对荧光蛋白偶联物、肽、核苷酸和核酸的荧光量子产率的检测进行了优化。百萤生物是AAT Bioquest的中国代理商,为您提供优质的荧光量子产率测定试剂盒 。
样品实验方案
表1
| 参考 | 水中的荧光量子产量 | 用以下染料或类似波长染料标记的缀合物(用于参考标准选择) |
| 参考1 | 0.98 | FAM, 6-TET, 6-HEX, 6-JOE, FITC, Cy®2, Alexa Fluor® 488 and 514, iFluor™ 488 and 514, DyLight™ 488, or other dyes that have an emission of 500 ± 50 nm |
| 参考2 | 0.20 | Cy3®, Alexa Fluor® 514, 532, 546 and 555, iFluor™ 514, 532 and 555, DyLight™ 555, TRITC, or other dyes that have an emission of 550 ± 50 nm |
| 参考3 | 0.44 | Texas Red®, Texas Red®-X, Alexa Fluor® 594, iFluor™ 594, California Red™, DyLight™ 594, or other dyes that have an emission of 600 ± 50 nm |
| 参考4 | 0.24 | Cy5®, Cy5.5®, Cy7®, Alexa Fluor® 633, 647, 700 and 750, iFluor™ 633, 647, 700 and 750, DyLight™ 650, 680 and 755, or other dyes that have an emission of 650 ± 50 nm |
所需的激发(nm)=较短的吸收值* - 50nm
*例如,如果您的测试样品在500 nm处具有吸收,并且所选参考标准在490 nm处具有吸收,则应选择440 nm(490 nm - 50 nm)作为激发波长。
1.从完全校准的荧光光谱计算荧光强度(参见仪器说明书)。
2.使用以下等式计算荧光量子产率:Φr = Φs * Ar/As
Φř和Φs分别为选择的参考标准和测试样品的荧光量子产率。Ar和As分别是所选参考标准品和测试样品的积分荧光强度(曲线面积)。

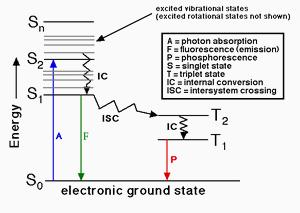
图1.荧光原理:电子被外源激发到更高的能级,返回到其基态后,将释放一定数量的光子,该光子与电子的能量损耗成比例地释放。 光子的释放表示荧光发射。荧光团的量子产率是其发射的光子与吸收的光子之比。
参考文献
Design of high-affinity peptide conjugates with optimized fluorescence quantum yield as markers for small peptide transporter PEPT1 (SLC15A1)
Authors: Bahadduri PM, Ray A, Khandelwal A, Swaan PW.
Journal: Bioorg Med Chem Lett (2008): 2555
Stability and fluorescence quantum yield of CdSe-ZnS quantum dots--influence of the thickness of the ZnS shell
Authors: Grabolle M, Ziegler J, Merkulov A, Nann T, Resch-Genger U.
Journal: Ann N Y Acad Sci (2008): 235
Fluorescence spectra and fluorescence quantum yield of sulfosalicylic acid
Authors: Wei YJ, Li N, Qin SJ.
Journal: Guang Pu Xue Yu Guang Pu Fen Xi (2004): 647
Measurement of fluorophore concentrations and fluorescence quantum yield in tissue-simulating phantoms using three diffusion models of steady-state spatially resolved fluorescence
Authors: Diamond KR, Farrell TJ, Patterson MS.
Journal: Phys Med Biol (2003): 4135
Fluorescence quantum yield determination of pyrimidine (6-4) pyrimidone photoadducts
Authors: Blais J, Douki T, Vigny P, Cadet J.
Journal: Photochem Photobiol (1994): 402
A comparison of three photosensitizers with respect to efficiency of cell inactivation, fluorescence quantum yield and DNA strand breaks
Authors: Kvam E, Moan J.
Journal: Photochem Photobiol (1990): 769
The fluorescence quantum yield of vitamin A2
Authors: Tsin AT, Pedrozo-Fernandez HA, Gallas JM, Chambers JP.
Journal: Life Sci (1988): 1379
Fluorescence decay and quantum yield characteristics of acridine orange and proflavine bound to DNA
Authors: Kubota Y, Steiner RF.
Journal: Biophys Chem (1977): 279
Dependence of the fluorescence quantum yield of complexes of acriflavine with tRNA on its structure
Authors: Borisova OF, Potapov AP, Surovaya AN, Trubitsin SN, Vol'kenshtein MV.
Journal: Mol Biol (1974): 411
5-dimethylaminonaphthalene-1-sulfonic acid (DANS acid) as standard for quantum yield of fluorescence
Authors: Himel CM, Mayer RT.
Journal: Anal Chem (1970): 130